RELATED PRODUCTS NOT AVAILABLE
true
Support
Formulaire de contact en ligne
Remplissez le formulaire
Merci d’avoir contacté notre équipe commerciale !
Un représentant commercial vous contactera sous peu.
Tous les contacts
Stent vasculaire couvert Covera™
le seul stent couvert indiqué pour les greffons AV et les fistules AV natives***

- Présentation
- Expérience clinique
- Products & Accessories
- Instructions d'utilisation et ressources
Le stent couvert conçu pour les patients nécessitant un accès AV
Le stent couvert vasculaire Covera™ s’appuie sur des technologies éprouvées du leader de la catégorie en matière d’accès AV. Ce stent couvert est conçu pour équilibrer la flexibilité et la résistance nécessaires pour traiter les lésions difficiles de l’arc céphalique terminal, aux segments basiliques du point d’oscillation, jusqu’à l’anastomose veineuse du greffon AV.
Les configurations évasées et droites permettent un dimensionnement et une adaptation précis à la paroi vasculaire, tandis qu’un système de délivrance à molette facile à utiliser, avec deux options de vitesse, offre un contrôle optimal à la mise en place.
Le stent couvert vasculaire Covera™ a démontré son efficacité dans deux essais cliniques distincts : l’un chez des patients dialysés avec des greffons AV et l’autre chez des patients dialysés avec des fistules AV.1
Force et flexibilité radiales
Architecture unique et flexible de l’endoprothèse de base conçue pour s’adapter au vaisseau natif dans les anatomies AV difficiles.


Configurations évasées et droites pour optimiser le débit hémodynamique au niveau de l’anastomose veineuse
- La configuration évasée est destinée à une utilisation dans les anatomies où le diamètre du vaisseau d’évacuation est supérieur à celui du vaisseau d’entrée
- La configuration droite est destinée à une utilisation dans des anatomies où le diamètre du vaisseau d’évacuation est inférieur ou égal à celui du vaisseau d’entrée

Embout atraumatique conçu pour faciliter l’insertion et le retrait au niveau du site d’accès
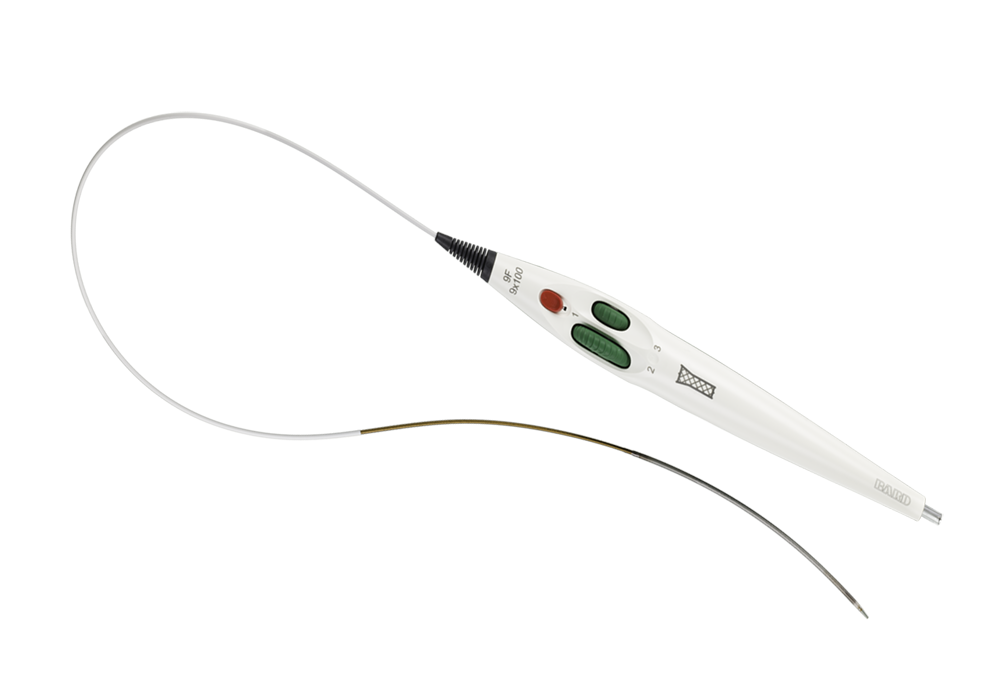
Facilite le contrôle précis de la mise en place
Système de mise en place triaxiale intuitif conçu pour une mise en place précise et pour faciliter une couverture optimale de la lésion
*** Aux États-Unis ,à compter de janvier 2023
1 Dolmatch B, Waheed U, Balamuthusamy S, Hoggard J, Settlage R; AVeVA Trial Investigators. Prospective, Multicenter Clinical Study of the Covera Vascular Covered Stent in the Treatment of Stenosis at the Graft-Vein Anastomosis of Dysfunctional Hemodialysis Access Grafts. J Vasc Interv Radiol. 2022;33(5):479-488.e3. doi:10.1016/j. jvir.2022.02.008. Données des études cliniques AVeNEW archivées. À 6 mois dans AVeVA, la perméabilité primaire de la lésion cible (TLPP) était de 70,3 % (analyse proportionnelle). À 6 mois dans AVeNEW, le TLPP était de 78,7 % pour l’endoprothèse vasculaire couverte Covera™ contre 47,9 % pour l’ATP seule, P < 0,001. 130 des 142 (91,5 %) sujets randomisés dans le groupe de l’endoprothèse vasculaire Covera™ et 123 sur les 138 (89,1 %) randomisés pour une ATP ont terminé leur suivi à 6 mois. Le TLPP est défini comme l’intervalle suivant l’intervention d’indexation jusqu’à la prochaine réintervention clinique sur ou à proximité du site de traitement d’origine ou jusqu’à ce que l’extrémité soit abandonnée pour un accès permanent. Dans AVeNEW, le TLPP à 6 mois – Analyse de sous-groupes est fournie sous forme de données observationnelles sans les valeurs de P. Dans AVeNEW, les patients qui ont reçu l’endoprothèse vasculaire couverte Covera™ ont subi 103 réinterventions impliquant une nouvelle lésion contre 72 réinterventions dans le groupe ATP uniquement à 24 mois. À 30 jours, l’absence d’événements de sécurité primaires était de 96,4 % dans l’AVeVa et de 95,0 % dans l’endoprothèse vasculaire couverte Covera™ contre 96,4 % (ATP seule) dans l’AVeNEW (P < 0,0022). L’absence d’événements de sécurité primaires a été définie comme l’absence d’événement indésirable impliquant le circuit d’accès ayant entraîné une intervention supplémentaire, une chirurgie, une hospitalisation ou le décès.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité.
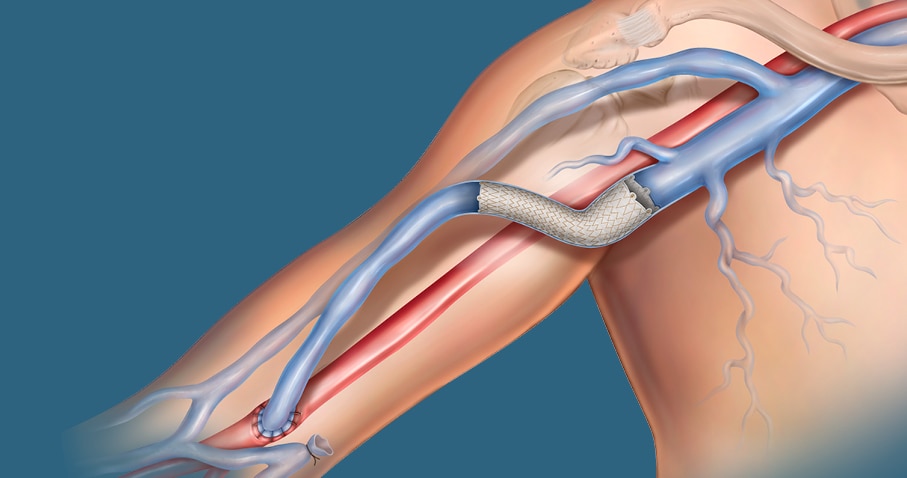
L’endoprothèse vasculaire couverte Covera™ a été conçue pour traiter les lésions difficiles dans le circuit d’accès AV, notamment l’arcade céphalique terminale, les segments basiliques de point oscillant et l’anastomose veine-greffon.
L’endoprothèse vasculaire couverte Covera™ a démontré son efficacité dans le cadre de deux essais cliniques distincts, l’un portant sur des patients sous dialyse avec des greffons AV et l’autre sur des patients sous dialyse avec des fistules AV ; tous deux ont démontré les avantages de la conception innovante de l’endoprothèse.1
AVeVA était une étude prospective, non randomisée, à un seul bras, multicentrique portant sur l’endoprothèse vasculaire couverte Covera™ utilisée pour traiter les sténoses au niveau de l’anastomose d’un greffon artério-veineux et d’une veine sortante. 110 patients ont été traités avec l’endoprothèse vasculaire couverte Covera™ dans 14 centres de recherche aux États-Unis
L’étude clinique AVeVA a démontré que l’endoprothèse vasculaire couverte Covera™ est efficace dans le traitement des sténoses au niveau de l’anastomose veine-greffon des patients sous dialyse avec un greffon AV.
| Méthodologie de l’étude | Prospective, multicentrique, à bras unique, non randomisée |
| Objectif | Évaluer la sécurité et l’efficacité de l’endoprothèse vasculaire couverte Covera™ dans le traitement des lésions sténosées au niveau de l’anastomose veine-greffon des patients sous hémodialyse dialysés avec un greffon AV |
| État | Suivi à 24 mois effectué |
| Nombre de patients/centres | 110 patients ont été traités avec l’endoprothèse vasculaire couverte Covera™ dans 14 centres de recherche aux États-Unis |
| Critère d’évaluation principal de l’efficacité | Perméabilité primaire de la lésion cible (TLPP) - 6 mois |
| Critère d’évaluation principal de la sécurité | Absence d’événement indésirable impliquant le circuit d’accès entraînant une intervention supplémentaire, une intervention chirurgicale, une hospitalisation ou un décès à 30 jours |
| Suivi | 30 et 90 jours ; 6, 12, 18 et 24 mois |
Perméabilité primaire de la lésion cible (TLPP) à 6 mois après le traitement des sténoses anastomotiques du greffon AV avec des greffons d’endoprothèse BD
Ce tableau est uniquement destiné à des fins de formation et non à des fins de comparaison. Les différences dans la méthodologie des études peuvent avoir un impact sur les résultats. Consulter les manuscrits complets pour connaître les détails complets de la méthodologie des études.
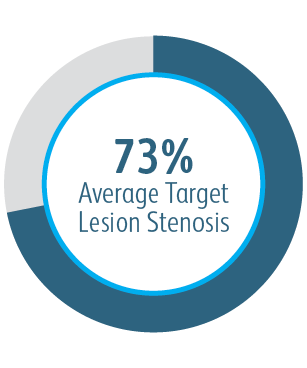
Dans l’étude clinique AVeVA, l’endoprothèse vasculaire couverte Covera™ a été étudiée auprès d’une cohorte de patients difficiles.
| Méthodologie de l’étude | Prospective, multicentrique, randomisée, à contrôle simultané |
| Objectif | Évaluer la sécurité et l’efficacité de l’endoprothèse vasculaire couverte Covera™ pour le traitement des lésions sténosées dans l’écoulement veineux des membres supérieurs du circuit d’accès AV des patients sous hémodialyse dialysés avec une fistule AV |
| État | Suivi à 24 mois effectué |
| Nombre de patients/centres | 280 sujets randomisés dans 24 centres de recherche (États-Unis, UE et ANZ) |
| Critère d’évaluation principal de l’efficacité | Perméabilité primaire de la lésion cible (TLPP) - 6 mois |
| Critère d’évaluation principal de la sécurité | Absence de tout événement de sécurité grave défini par le protocole impliquant le circuit d’accès AV pendant 30 jours |
| Suivi | À la sortie de l’hôpital, 30 et 90 jours ; 6, 12, 18 et 24 mois |
Au cours de l’étude clinique AVeNEW, l’endoprothèse vasculaire couverte Covera™ a été utilisée dans le traitement d’une population de patients difficiles présentant des caractéristiques de lésions difficiles.
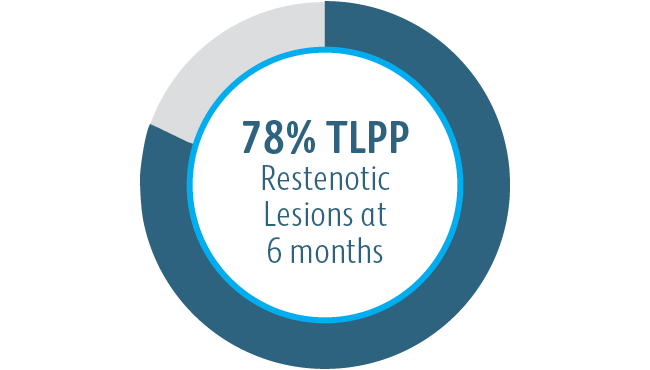
À 6 et 12 mois, l’endoprothèse vasculaire couverte Covera™ était supérieure au groupe de contrôle de l’ATP en ce qui concerne le traitement des sténoses dans l’écoulement veineux de patients dialysés avec une fistule artérioveineuse.
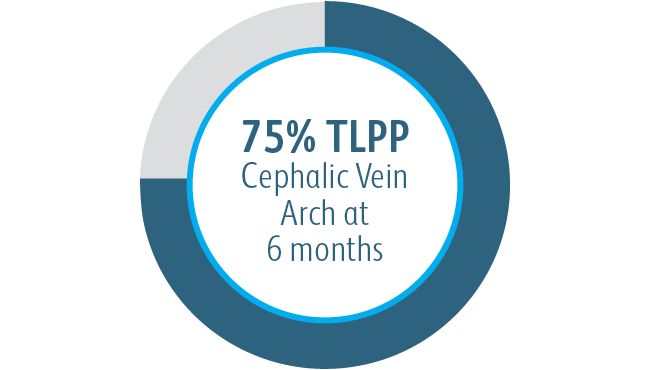
Tous les sous-groupes ont montré des bénéfices à 6 mois
Dans tous les sous-groupes de localisation des lésions cibles analysés, l’endoprothèse vasculaire couverte Covera™ a démontré une plus grande perméabilité primaire de la lésion cible par rapport à l’ATP seule, y compris ceux traités au niveau de l’arcade de la veine céphalique.
Critères d’évaluation supplémentaires de l’étude clinique AVeNEW
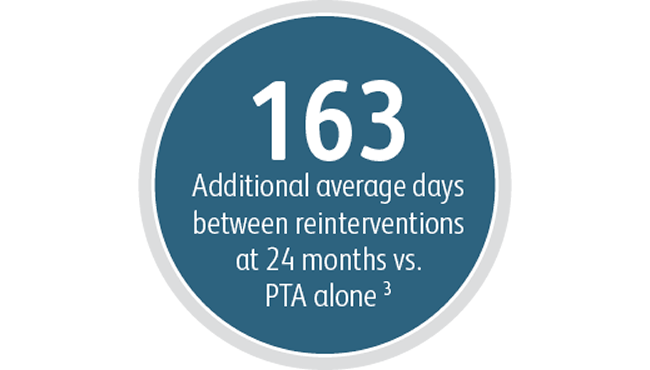
Outre les avantages pour la perméabilité primaire de la lésion cible, l’endoprothèse vasculaire couverte Covera™ a démontré un degré élevé de réussite technique aiguë et prolongé la durée moyenne entre les interventions sur la lésion cible par rapport à l’ATP seule.
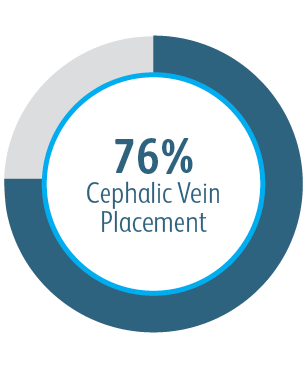
Au cours de l’étude clinique AVeNEW, 77 patients présentant des sténoses dans l’arcade de la veine céphalique ont été traités avec
l’endoprothèse vasculaire couverte Covera™.
Dans cet exemple, l’angiographie de référence montre le rétrécissement vasculaire et la réussite technique aiguë avec restauration du vaisseau et conformabilité de l’endoprothèse couverte.
* Haskal ZJ, Trerotola S, Dolmatch B, et al. Stent graft versus balloon angioplasty for failing dialysis-access grafts. N Engl J Med. 2010 Feb 11;362(6):494-503.
** Haskal ZJ, Saad TF, Hoggard JG, et al. Prospective, randomized, concurrently-controlled study of a stent graft versus balloon angioplasty for treatment of arteriovenous access graft stenosis: 2-year results of the RENOVA study. J Vasc Interv Radiol. 2016 Aug;27(8):1105-1114.e3.
***Aux États-Unis en novembre 2022
1 Dolmatch B, Waheed U, Balamuthusamy S, Hoggard J, Settlage R; AVeVA Trial Investigators. Prospective, multicenter clinical study of the Covera Vascular Covered Stent in the treatment of stenosis at the graft-vein anastomosis of dysfunctional hemodialysis access grafts. J Vasc Interv Radiol. 2022;33(5):479-488.e3. doi:10.1016/j. jvir.2022.02.008. Données des études cliniques AVeNEW archivées. À 6 mois dans AVeVA, la perméabilité primaire de la lésion cible (TLPP) était de 70,3 % (analyse proportionnelle). À 6 mois dans AVeNEW, le TLPP était de 78,7 % pour l’endoprothèse vasculaire couverte Covera™ contre 47,9 % pour l’ATP seule, P < 0,001. 130 des 142 (91,5 %) sujets randomisés dans le groupe de l’endoprothèse vasculaire Covera™ et 123 sur les 138 (89,1 %) randomisés pour une ATP ont terminé leur suivi à 6 mois. Le TLPP est défini comme l’intervalle suivant l’intervention d’indexation jusqu’à la prochaine réintervention clinique sur ou à proximité du site de traitement d’origine ou jusqu’à ce que l’extrémité soit abandonnée pour un accès permanent. Dans AVeNEW, le TLPP à 6 mois – Analyse de sous-groupes est fournie sous forme de données observationnelles sans les valeurs de P. Dans AVeNEW, les patients qui ont reçu l’endoprothèse vasculaire couverte Covera™ ont subi 103 réinterventions impliquant une nouvelle lésion contre 72 réinterventions dans le groupe ATP uniquement à 24 mois. À 30 jours, l’absence d’événements de sécurité primaires était de 96,4 % dans l’AVeVa et de 95,0 % dans l’endoprothèse vasculaire couverte Covera™ contre 96,4 % (ATP seule) dans l’AVeNEW (P < 0,0022). L’absence d’événements de sécurité primaires a été définie comme l’absence d’événement indésirable impliquant le circuit d’accès ayant entraîné une intervention supplémentaire, une chirurgie, une hospitalisation ou le décès.
2 La réussite technique aiguë a été définie comme le déploiement réussi de l’implant à l’endroit prévu, de l’avis de l’utilisateur, évalué au moment de la procédure d’indexation. Étude clinique AVeNEW. Données archivées. Bard Peripheral Vascular Inc., Tempe, AZ.
3 L’indice de perméabilité fonctionnelle – Lésion cible (IPF-T) a été défini comme le temps écoulé entre la procédure d’indexation de l’étude et l’abandon complet de l’accès, divisé par le nombre de visites pour une nouvelle intervention réalisée au niveau de la lésion cible afin de préserver l’accès vasculaire pour l’hémodialyse. IPF-T moyen de 380,40 jours avec l’endoprothèse vasculaire couverte Covera™ contre 217,57 jours avec l’ATP seule à 24 mois. Étude clinique AVeNEW. Données archivées. Bard Peripheral Vascular Inc., Tempe, AZ.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité.
BD-23522v2
Publications
Pour accompagner votre démarche d’amélioration continue, BD référence de nombreuses publications utilisant ses solutions.
En savoir plus
Formation
BD propose des programmes de formation pour vous aider à améliorer vos pratiques cliniques, dans le cadre de notre objectif : faire progresser le monde de la santé.
En savoir plus
Événements
BD aide le secteur de la santé en proposant des produits et des services de pointe pour améliorer les soins tout en diminuant les coûts. Nous organisons des événements et participons à des rencontres conformément à notre engagement : Faire progresser le monde de la santé™.
En savoir plus
Études de cas
BD favorise l’excellence clinique en proposant un large éventail de ressources sur les bonnes pratiques, les innovations et les tendances du secteur de la santé.
En savoir plus
true
true