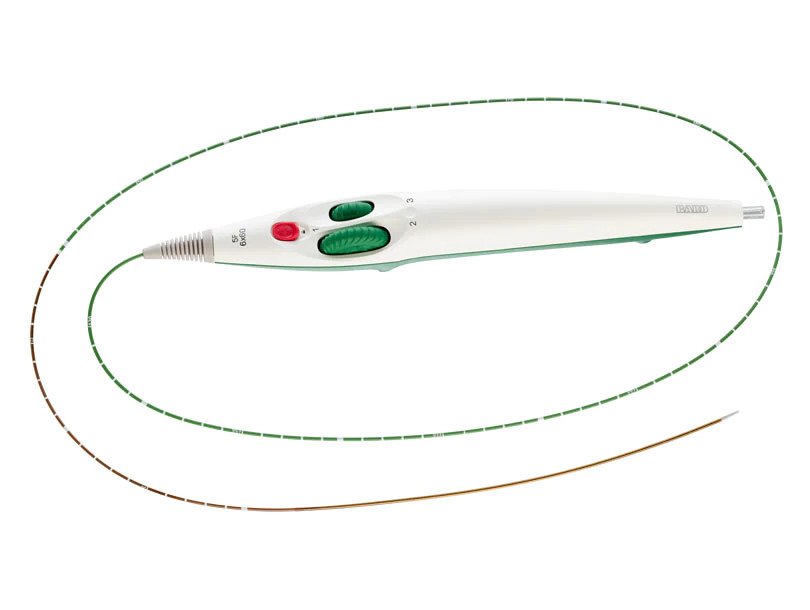
- Conception hélicoïdale unique conçue pour la flexion, la compression et la torsion
- Seul stent approuvé par la FDA pour l’artère fémorale superficielle (SFA) et l’artère poplitée dans son intégralité¹
- Système de délivrance à profil bas de 5F
- Déploiement à double vitesse par molette, conçu pour faciliter l’utilisation et garantir une précision de placement²
- Système de marquage GeoAlign™ conçu pour améliorer l’efficacité de la procédure et réduire l’exposition aux rayonnements³





- Présentation
- Products & Accessories
- Instructions d'utilisation et ressources
Conception prouvée dans le cadre d'essais clinique :
« Seule endoprothèse disponible dans le commerce approuvée par la FDA pour l’artère fémorale superficielle et l’artère poplitée complète, le stent LifeStent™ s’est taillé une réputation de haute performance :
- Dans le cadre d’une étude RESILIENT de niveau 1 , le stent LifeStent™ a démontré la supériorité de son traitement par rapport à l’angioplastie par ballonnet avec une efficacité soutenue pendant 3 ans4
- Dans l’étude ETAP de niveau 1 menée à l’initiative de l’investigateur sur l’artère poplitée, le stent LifeStent™ a démontré un taux de perméabilité primaire deux fois supérieur à celui de l’ATP pendant deux ans5
- Lors d’une évaluation clinique du traitement sur des lésions longues, le stent LifeStent™ a démontré une perméabilité primaire élevée à 12 mois pour des lésions mesurant jusqu’à 240 mm6
Le stent LifeStent™, dans diverses tailles, ont été étudiés dans le cadre de plus de dix essais cliniques à l’échelle mondiale.7
Le système d’endoprothèse vasculaire LifeStent™ 5F offre la même conception d’endoprothèse hélicoïdale avancée cliniquement éprouvée que l’endoprothèse vasculaire LifeStent™ sur un système de mise en place de 5 F de petite taille. Le système de mise en place de 5 F LifeStent™ permet un déploiement à double vitesse par molette avec un cathéter tri-axial conçu pour faciliter l’utilisation, le contrôle du déploiement et la précision du positionnement.2
Le système d’endoprothèse vasculaire de 5 F LifeStent™ fait partie de BD Halo Effect, une suite de produits de petite taille conçus pour minimiser la taille de l’artériotomie et permettre aux médecins d’effectuer une procédure 5F lors du traitement de l’AFS et de l’artère poplitée. La suite BD Halo Effect comprend également :
Le système d’endoprothèse vasculaire Le système de graduations GeoAlign™ est présent sur tous les produits comprend le système de graduations GeoAlign™, une règle non radio-opaque simple à utiliser située sur le corps du cathéter. Le système de graduations GeoAlign™ est présent sur tous les produits Bard 5F ProSeries™. Le système de graduations GeoAlign™ est conçu pour faciliter l’alignement répétable du cathéter au niveau de la lésion et augmenter l’efficacité de la procédure en minimisant l’exposition à la radioscopie.3
Endoprothèse périphérique destinée à améliorer le diamètre luminal
Le système d’endoprothèse vasculaire LifeStent™ 5F est une endoprothèse périphérique destinée à améliorer le diamètre luminal dans le traitement des lésions symptomatiques de-novo ou resténotiques de l’artère fémorale superficielle (AFS) native et de l’artère poplitée. Le système d’endoprothèse vasculaire LifeStent™ 5F est disponible en diamètres de 5 mm, 6 mm et 7 mm, et en longueurs de 20 mm à 170 mm. Se reporter au tableau des spécifications pour les options de taille spécifiques.
1 Commercially available as of December 2023
2 Based on physician ratings during animal testing. May not be indicative of clinical performance. Data on file at Bard Peripheral Vascular, Inc., Tempe, AZ.
3 The GeoAlign™ Marking System provides an approximation that may not be an exact representation of the distance traveled intravascularly and should be confirmed under fluoroscopy.
4 Freedom from TLR at 3 years: 75.5% LifeStent™ Vascular Stent arm (n=134), 41.8% PTA arm (n=72), p LifeStent™ Vascular Stent in 6 mm and 7 mm diameters and lengths of 40-80 mm. The LifeStent™ 5 mm stent diameter and LifeStent™ 5F delivery system were not included in these clinical studies.
5 Primary Patency at 2 years: 64.2% LifeStent™ Vascular Stent arm (n=89), 31.3% PTA arm (n=94), p=0.0001. Patency rates calculated when provisional stenting is considered TLR. Kaplan-Meier analysis with Mantel-Cox log-rank test. The study included LifeStent™ Vascular Stent in 6 mm, 7 mm and 8 mm diameters and lengths of 20-170 mm. The LifeStent™ 5 mm stent diameter and LifeStent™ 5F delivery system were not included in these clinical studies.
6 Primary Patency at 12 months: 81.5% all lesion lengths (n=53). This study included LifeStent™ Vascular Stent in 6 mm and 7 mm diameters and lengths of 20-200 mm. The LifeStent™ 5 mm stent diameter and LifeStent™ 5F delivery system were not included in these clinical studies.
Please consult Instructions for Use under Resources for product indications for use, contraindications, warnings, precautions, complications, adverse events and detailed safety information.
BD-23527v2
Pour accompagner votre démarche d’amélioration continue, BD référence de nombreuses publications utilisant ses solutions.
BD propose des programmes de formation pour vous aider à améliorer vos pratiques cliniques, dans le cadre de notre objectif : faire progresser le monde de la santé.
BD aide le secteur de la santé en proposant des produits et des services de pointe pour améliorer les soins tout en diminuant les coûts. Nous organisons des événements et participons à des rencontres conformément à notre engagement : Faire progresser le monde de la santé™.
BD favorise l’excellence clinique en proposant un large éventail de ressources sur les bonnes pratiques, les innovations et les tendances du secteur de la santé.
Veuillez noter que certains produits, services ou caractéristiques pourraient ne pas être disponibles dans votre région. Veuillez consulter votre représentant BD local.
- Commercialisation à partir de décembre 2020
- Sur la base de notes des médecins au cours d’essais sur des animaux. N’est pas forcément indicatif de la performance clinique réelle. Données archivées auprès de Bard Peripheral Vascular, Inc., Tempe, AZ.
- Le système de graduations GeoAlign™ fournit une approximation qui peut ne pas être une représentation exacte de la distance parcourue par voie intravasculaire et doit être confirmée sous radioscopie.
- Absence de TLR à 3 ans : bras traité par l’endoprothèse vasculaire LifeStent™ 75,5 % (n = 134), bras traité par ATP 41,8 % (n = 72), endoprothèse vasculaire p LifeStent™ en diamètres de 6 mm et 7 mm et longueurs de 40 à 80 mm. L’endoprothèse LifeStent™ de 5 mm et le système de mise en place LifeStent™ 5F n’ont pas été inclus dans ces études cliniques.
- Perméabilité primaire à 2 ans : bras traité par l’endoprothèse vasculaire LifeStent™ 64,2 % (n = 89), bras traité par ATP 31,3 % (n = 94), p = 0,0001. Taux de perméabilité calculés lorsque la pose provisoire d’une endoprothèse est considérée comme une revascularisation de la lésion cible. Analyse Kaplan-Meier au moyen du test logarithmique par rangs Mantel-Cox. L’étude incluait des endoprothèses vasculaires LifeStent™ de 6 mm, 7 mm et 8 mm de diamètre et des longueurs de 20 à 170 mm. L’endoprothèse LifeStent™ de 5 mm de diamètre et le système de mise en place LifeStent™ 5F n’ont pas été inclus dans ces études cliniques.
- Perméabilité primaire à 12 mois : 81,5 % sur les lésions de toutes longueurs (n = 53). Cette étude incluait des endoprothèses vasculaires LifeStent™ de 6 mm et 7 mm de diamètre et de 20 à 200 mm de longueur. Des endoprothèses LifeStent™ de 5 mm de diamètre et le système de mise en place LifeStent™ 5F n’ont pas été inclus dans ces études cliniques.
- Essais RESILIENT I/II, essai E-TAGIUSS, essai STELLA, analyse rétrospective des endoprothèses vasculaires LifeStent™ dans le traitement des lésions à segments longs, étude sur le système de mise en place d’endoprothèses vasculaires LifeStent™ (essai LifeStent™ 200 mm), essai CONTINUUM, essais REALITY I/II/III, essai ETAP et essai RELIABLE.
Lire le mode d’emploi pour connaître les indications d’utilisation, les contre-indications, les avertissements, les précautions, les complications, les événements indésirables et les informations détaillées sur la sécurité.